Pada 24 Agustus 2021, Cara Therapeutics dan mitra bisnisnya, Vifor Pharma, mengumumkan bahwa agonis reseptor opioid kappa pertama di kelasnya, difelikefalin (KORSUVA™), telah disetujui oleh FDA untuk pengobatan pasien penyakit ginjal kronis (PGK) (pruritus sedang/berat positif dengan terapi hemodialisis). Produk ini diperkirakan akan diluncurkan pada kuartal pertama 2022. Cara dan Vifor menandatangani perjanjian lisensi eksklusif untuk komersialisasi KORSUVA™ di Amerika Serikat dan sepakat untuk menjual KORSUVA™ kepada Fresenius Medical. Di antara mereka, Cara dan Vifor masing-masing memiliki 60% dan 40% bagi hasil penjualan dari Fresenius Medical; masing-masing memiliki 50% bagi hasil penjualan dari Fresenius Medical.
Pruritus terkait CKD (CKD-aP) adalah pruritus umum yang terjadi dengan frekuensi dan intensitas tinggi pada pasien CKD yang menjalani dialisis. Pruritus terjadi pada sekitar 60%-70% pasien yang menjalani dialisis, dengan 30%-40% di antaranya mengalami pruritus sedang/berat, yang sangat memengaruhi kualitas hidup (misalnya, kualitas tidur yang buruk) dan berhubungan dengan depresi. Belum ada pengobatan yang efektif untuk pruritus terkait CKD, dan persetujuan Difelikefalin membantu mengatasi kesenjangan kebutuhan medis yang besar. Persetujuan ini didasarkan pada dua uji klinis Fase III penting dalam pengajuan NDA: data positif dari uji klinis KALM-1 dan KALM-2 di AS dan global, dan data pendukung dari 32 studi klinis tambahan, yang menunjukkan bahwa KORSUVA™ dapat ditoleransi dengan baik.
Belum lama ini, kabar baik datang dari studi klinis difelikefalin di Jepang: pada 10 Januari 2022, Cara mengumumkan bahwa mitranya, Maruishi Pharma dan Kissey Pharma, mengonfirmasi bahwa injeksi difelikefalin digunakan di Jepang untuk pengobatan pruritus pada pasien hemodialisis. Uji klinis fase III menunjukkan titik akhir primer terpenuhi. Sebanyak 178 pasien menerima difelikefalin atau plasebo selama 6 minggu dan berpartisipasi dalam studi perpanjangan label terbuka selama 52 minggu. Titik akhir primer (perubahan skor skala penilaian numerik pruritus) dan titik akhir sekunder (perubahan skor gatal pada Skala Keparahan Shiratori) menunjukkan perbaikan yang signifikan dari awal pada kelompok difelikefalin dibandingkan dengan kelompok plasebo dan ditoleransi dengan baik.
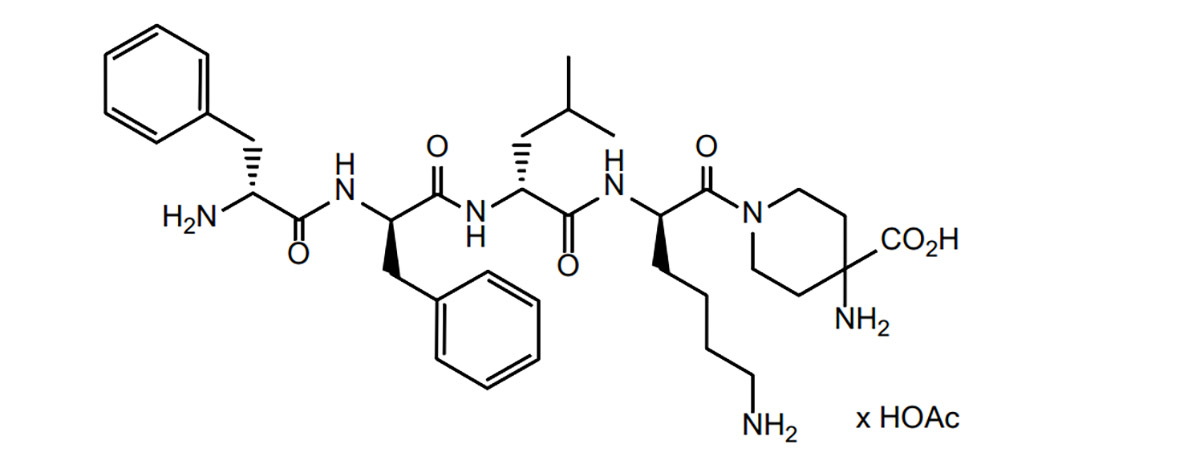
Difelikefalin adalah golongan peptida opioid. Berdasarkan hal ini, Peptide Research Institute telah mempelajari literatur tentang peptida opioid, dan merangkum kesulitan dan strategi peptida opioid dalam pengembangan obat, serta situasi pengembangan obat saat ini.
Waktu posting: 17-Feb-2022